فهرست مطالب:

تصویری: فرم 510k چیست؟
2024 نویسنده: Stanley Ellington | [email protected]. آخرین اصلاح شده: 2023-12-16 00:16
آ 510 (k ) ارسالی حاوی اطلاعات مورد نیاز تحت 21 CFR 807.87 است. برای کسب اطلاعات بیشتر در مورد چارچوب نظارتی، سیاست ها، و شیوه های زیربنایی FDA 510(k ) بررسی، لطفا به راهنمایی مراجعه کنید 510(k ) برنامه: ارزیابی معادل سازی اساسی در اطلاع رسانی قبل از بازار [ 510(k )].
علاوه بر این، پرونده 510k چیست؟
آ 510 (K ) یک پیش بازار است ارسال ساخته شده برای FDA برای نشان دادن اینکه دستگاهی که باید به بازار عرضه شود حداقل به همان اندازه ایمن و مؤثر است، یعنی تقریباً معادل دستگاهی است که به طور قانونی به بازار عرضه شده است (21 CFR §807.92(a)(3)) که مشمول تأیید قبل از بازار نیست. پایگاه داده جستجو بیشتر بیاموزید. راهنما دانلود فایل ها. 510 هزار
به همین ترتیب، 510k ویژه چیست؟ ویژه 510(k )s اجازه می دهد FDA و صنعت باید به بررسی قبلی آژانس در مورد اطلاعات دقیق، در صورت لزوم، بدون تغییر الزامات قانونی یا نظارتی مربوط به فرآیند اعلان قبل از بازار طبق بخشهای 510 و 513 قانون FD&C و 21 CFR 807 زیربخش E، تکیه کند.
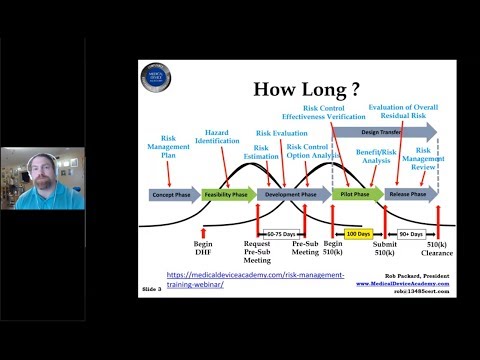
از این رو، چگونه یک 510 K را تهیه می کنید؟
برای شروع، در اینجا لیستی از تمام بخش های مورد نیاز برای ارسال 510(k) آمده است:
- گروه 1 - فرم های برگه جلد.
- گروه 2 - آنچه دیگران می توانند ببینند.
- گروه 3 - بخش های قالب.
- گروه 4 - مقایسه محصول شما با محمول(های)
- گروه 5 - تضمین ایمنی بیمار.
- گروه 6 - نرم افزار و الکترونیک.
- گروه 7 - تست عملکرد.
تفاوت بین 510k و PMA چیست؟
آ PMA عمیق تر از الف است 510 هزار - برای اثبات اینکه یک دستگاه جدید برای کاربر نهایی ایمن و مؤثر است و معمولاً به آزمایشهای بالینی با شرکتکنندگان انسانی همراه با آزمایشهای آزمایشگاهی نیاز دارد، استفاده میشود.
توصیه شده:
فرم 216 چیست؟

فرم 216. هدف: فرم 216 در مورد 1-4 املاک سرمایه گذاری درآمدی و 2-4 املاک تحت اشغال خانواده استفاده می شود. توضیحات: متقاضی پیش بینی درآمد و هزینه را ارائه می دهد تا در تعیین رویکرد درآمد به ارزش مورد استفاده قرار گیرد
ورودی مجله پیش فرم چیست؟

در حسابداری مالی ، پیش فرم به گزارش سود شرکت اشاره می کند که معاملات غیرمعمول یا غیر تکراری را شامل نمی شود. هزینه های مستثنی می تواند شامل کاهش ارزش سرمایه گذاری ، هزینه های بازسازی و تعدیلات موجود در ترازنامه شرکت باشد که خطاهای حسابداری سالهای گذشته را برطرف می کند
فرم ارزیابی 1025 چیست؟

فرم 1025 مارس 2005 Fannie Mae. هدف از این گزارش ارزیابی خلاصه ارائه نظر دقیق و با پشتیبانی کافی در مورد ارزش بازار ملک موضوع به وام دهنده/مشتری است
فرم کامل SRM چیست؟

نوع مدرسه: دانشگاه فرضی
فرم سفارش داخلی چیست؟

سفارش داخلی یک پروژه کوچک مستقل است که به عنوان مجموعه ای از هزینه ها کار می کند. مشاهده الگوی فرم سفارش داخلی در مشاغل یک اتفاق بسیار رایج است که بیشتر در ادارات اتفاق می افتد. سفارشات داخلی را می توان در فرمت های بسیاری مانند PDF و Word ذخیره کرد
